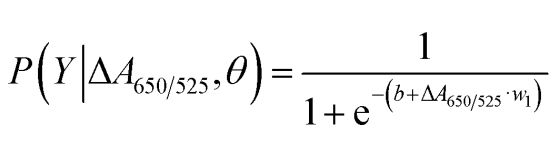ການກວດຫາມະເຮັງແຕ່ຫົວທີໂດຍອີງໃສ່ການກວດເນື້ອເຍື່ອດ້ວຍນ້ຳແມ່ນທິດທາງໃໝ່ຂອງການກວດຫາ ແລະ ການວິນິດໄສມະເຮັງທີ່ສະເໜີໂດຍສະຖາບັນມະເຮັງແຫ່ງຊາດສະຫະລັດໃນຊຸມປີມໍ່ໆມານີ້, ໂດຍມີຈຸດປະສົງເພື່ອກວດຫາມະເຮັງໃນໄລຍະຕົ້ນ ຫຼື ແມ່ນແຕ່ເນື້ອງອກກ່ອນເປັນມະເຮັງ. ມັນໄດ້ຖືກນໍາໃຊ້ຢ່າງກວ້າງຂວາງເປັນຕົວຊີ້ວັດທາງຊີວະພາບໃໝ່ສໍາລັບການວິນິດໄສພະຍາດຮ້າຍຕ່າງໆໃນໄລຍະຕົ້ນ, ລວມທັງມະເຮັງປອດ, ເນື້ອງອກໃນກະເພາະອາຫານ, ເນື້ອງອກໃນຕ່ອມລູກໝາກ ແລະ ເນື້ອງອກທາງພະຍາດຍິງ.
ການເກີດຂຶ້ນຂອງເວທີເພື່ອລະບຸຕົວຊີ້ວັດທາງຊີວະພາບພູມສັນຖານເມທິເລຊັນ (Methylscape) ມີທ່າແຮງທີ່ຈະປັບປຸງການກວດຫາມະເຮັງໃນໄລຍະຕົ້ນໆທີ່ມີຢູ່ແລ້ວຢ່າງຫຼວງຫຼາຍ, ເຮັດໃຫ້ຄົນເຈັບຢູ່ໃນໄລຍະທີ່ສາມາດປິ່ນປົວໄດ້ໄວທີ່ສຸດ.
ເມື່ອບໍ່ດົນມານີ້, ນັກຄົ້ນຄວ້າໄດ້ພັດທະນາແພລດຟອມການຮັບຮູ້ທີ່ງ່າຍດາຍ ແລະ ໂດຍກົງສຳລັບການກວດຫາພູມສັນຖານເມທິເລຊັນໂດຍອີງໃສ່ອະນຸພາກຄຳທີ່ປະດັບດ້ວຍຊີສເຕອາມີນ (Cyst/AuNPs) ລວມກັບເຊັນເຊີຊີວະພາບທີ່ອີງໃສ່ໂທລະສັບສະຫຼາດ ເຊິ່ງຊ່ວຍໃຫ້ສາມາດກວດຫາເນື້ອງອກໄດ້ໄວໃນໄລຍະຕົ້ນໆ. ການກວດຫາມະເຮັງເມັດເລືອດຂາວໃນໄລຍະຕົ້ນໆສາມາດເຮັດໄດ້ພາຍໃນ 15 ນາທີຫຼັງຈາກການສະກັດ DNA ຈາກຕົວຢ່າງເລືອດ, ດ້ວຍຄວາມຖືກຕ້ອງ 90.0%. ຫົວຂໍ້ບົດຄວາມແມ່ນການກວດຫາ DNA ມະເຮັງໃນເລືອດຂອງມະນຸດຢ່າງໄວວາໂດຍໃຊ້ AuNPs ທີ່ປິດດ້ວຍຊີສເຕອາມີນ ແລະ ໂທລະສັບສະຫຼາດທີ່ເປີດໃຊ້ການຮຽນຮູ້ຂອງເຄື່ອງຈັກ.
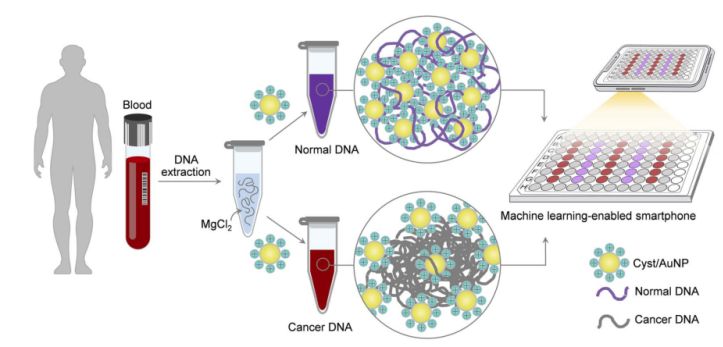
ຮູບທີ 1. ແພລດຟອມການຮັບຮູ້ທີ່ງ່າຍດາຍ ແລະ ໄວສຳລັບການກວດຫາມະເຮັງຜ່ານອົງປະກອບ Cyst/AuNPs ສາມາດເຮັດໄດ້ໃນສອງຂັ້ນຕອນງ່າຍໆ.
ນີ້ສະແດງຢູ່ໃນຮູບທີ 1. ກ່ອນອື່ນໝົດ, ສານລະລາຍທີ່ມີນໍ້າຖືກນໍາໃຊ້ເພື່ອລະລາຍຊິ້ນສ່ວນ DNA. ຫຼັງຈາກນັ້ນ, Cyst/AuNPs ໄດ້ຖືກເພີ່ມເຂົ້າໃນສານລະລາຍທີ່ປະສົມ. DNA ປົກກະຕິ ແລະ DNA ມະເຮັງມີຄຸນສົມບັດການເມທິເລຊັນທີ່ແຕກຕ່າງກັນ, ເຊິ່ງສົ່ງຜົນໃຫ້ຊິ້ນສ່ວນ DNA ມີຮູບແບບການປະກອບຕົວທີ່ແຕກຕ່າງກັນ. DNA ປົກກະຕິລວມຕົວກັນຢ່າງວ່າງໆ ແລະ ໃນທີ່ສຸດກໍ່ລວມຕົວກັນເປັນ Cyst/AuNPs, ເຊິ່ງສົ່ງຜົນໃຫ້ Cyst/AuNPs ມີລັກສະນະປ່ຽນສີແດງ, ດັ່ງນັ້ນການປ່ຽນແປງສີຈາກສີແດງເປັນສີມ່ວງສາມາດສັງເກດເຫັນໄດ້ດ້ວຍຕາເປົ່າ. ໃນທາງກົງກັນຂ້າມ, ໂປຣໄຟລ໌ການເມທິເລຊັນທີ່ເປັນເອກະລັກຂອງ DNA ມະເຮັງນໍາໄປສູ່ການຜະລິດກຸ່ມຊິ້ນສ່ວນ DNA ທີ່ໃຫຍ່ກວ່າ.
ຮູບພາບຂອງແຜ່ນ 96 ຫຼຸມຖືກຖ່າຍໂດຍໃຊ້ກ້ອງຖ່າຍຮູບໂທລະສັບສະຫຼາດ. DNA ຂອງມະເຮັງໄດ້ຖືກວັດແທກໂດຍໂທລະສັບສະຫຼາດທີ່ມີການຮຽນຮູ້ຂອງເຄື່ອງຈັກເມື່ອທຽບກັບວິທີການທີ່ອີງໃສ່ສະເປກໂຕຣສະໂຄປີ.
ການກວດຫາມະເຮັງໃນຕົວຢ່າງເລືອດຕົວຈິງ
ເພື່ອຂະຫຍາຍປະໂຫຍດຂອງແພລດຟອມການຮັບຮູ້, ນັກຄົ້ນຄວ້າໄດ້ນຳໃຊ້ເຊັນເຊີທີ່ຈຳແນກລະຫວ່າງ DNA ປົກກະຕິ ແລະ DNA ມະເຮັງໃນຕົວຢ່າງເລືອດຕົວຈິງໄດ້ຢ່າງສຳເລັດຜົນ. ຮູບແບບການເມທິເລຊັນຢູ່ບໍລິເວນ CpG ຄວບຄຸມການສະແດງອອກຂອງ gene ທາງ epigenetic. ໃນເກືອບທຸກປະເພດຂອງມະເຮັງ, ການປ່ຽນແປງໃນການເມທິເລຊັນ DNA ແລະດັ່ງນັ້ນໃນການສະແດງອອກຂອງ gene ທີ່ສົ່ງເສີມການເກີດຂອງເນື້ອງອກໄດ້ຖືກສັງເກດເຫັນວ່າສະຫຼັບກັນ.
ໃນຖານະເປັນຕົວແບບສຳລັບມະເຮັງອື່ນໆທີ່ກ່ຽວຂ້ອງກັບການເມທິເລຊັນ DNA, ນັກຄົ້ນຄວ້າໄດ້ໃຊ້ຕົວຢ່າງເລືອດຈາກຄົນເຈັບທີ່ເປັນມະເຮັງເມັດເລືອດຂາວ ແລະ ກຸ່ມຄວບຄຸມທີ່ມີສຸຂະພາບແຂງແຮງເພື່ອສືບສວນປະສິດທິພາບຂອງພູມສັນຖານເມທິເລຊັນໃນການຈຳແນກມະເຮັງເມັດເລືອດຂາວ. ເຄື່ອງໝາຍຊີວະພາບພູມສັນຖານເມທິເລຊັນນີ້ບໍ່ພຽງແຕ່ມີປະສິດທິພາບດີກວ່າວິທີການກວດຫາມະເຮັງເມັດເລືອດຂາວແບບໄວທີ່ມີຢູ່ແລ້ວເທົ່ານັ້ນ, ແຕ່ຍັງສະແດງໃຫ້ເຫັນເຖິງຄວາມເປັນໄປໄດ້ໃນການຂະຫຍາຍໄປສູ່ການກວດພົບມະເຮັງຫຼາກຫຼາຍຊະນິດໂດຍໃຊ້ການວິເຄາະທີ່ງ່າຍດາຍ ແລະ ຊັດເຈນນີ້.
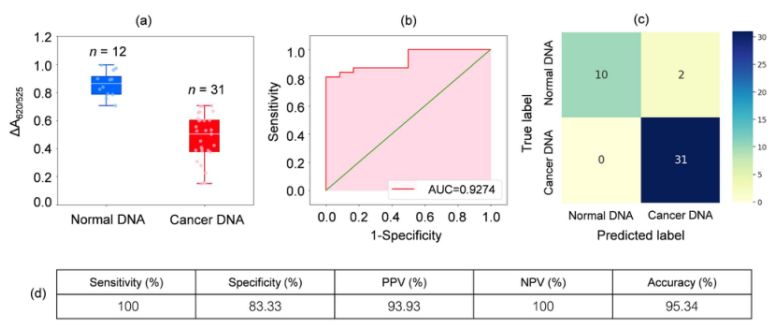
DNA ຈາກຕົວຢ່າງເລືອດຈາກຄົນເຈັບມະເຮັງເມັດເລືອດຂາວ 31 ຄົນ ແລະ ບຸກຄົນທີ່ມີສຸຂະພາບແຂງແຮງ 12 ຄົນໄດ້ຖືກວິເຄາະ. ດັ່ງທີ່ສະແດງຢູ່ໃນຕາຕະລາງໃນຮູບທີ 2a, ການດູດຊຶມທຽບເທົ່າຂອງຕົວຢ່າງມະເຮັງ (ΔA650/525) ແມ່ນຕໍ່າກວ່າ DNA ຈາກຕົວຢ່າງປົກກະຕິ. ນີ້ແມ່ນສ່ວນໃຫຍ່ແມ່ນຍ້ອນ hydrophobicity ທີ່ເພີ່ມຂຶ້ນເຊິ່ງນໍາໄປສູ່ການລວມຕົວຢ່າງໜາແໜ້ນຂອງ DNA ມະເຮັງ, ເຊິ່ງປ້ອງກັນການລວມຕົວຂອງ Cyst/AuNPs. ດັ່ງນັ້ນ, ອະນຸພາກເຫຼົ່ານີ້ຈຶ່ງກະແຈກກະຈາຍຢ່າງສົມບູນໃນຊັ້ນນອກຂອງກ້ອນມະເຮັງ, ເຊິ່ງສົ່ງຜົນໃຫ້ມີການກະຈາຍຕົວທີ່ແຕກຕ່າງກັນຂອງ Cyst/AuNPs ທີ່ດູດຊຶມຢູ່ໃນກ້ອນ DNA ປົກກະຕິ ແລະ ກ້ອນ DNA ມະເຮັງ. ຫຼັງຈາກນັ້ນ, ເສັ້ນໂຄ້ງ ROC ໄດ້ຖືກສ້າງຂຶ້ນໂດຍການປ່ຽນແປງຂອບເຂດຈາກຄ່າຕໍ່າສຸດຂອງ ΔA650/525 ໄປຫາຄ່າສູງສຸດ.
ຮູບທີ 2.(ກ) ຄ່າການດູດຊຶມທຽບເທົ່າຂອງສານລະລາຍ cyst/AuNPs ທີ່ສະແດງໃຫ້ເຫັນເຖິງການມີ DNA ປົກກະຕິ (ສີຟ້າ) ແລະ ມະເຮັງ (ສີແດງ) ພາຍໃຕ້ເງື່ອນໄຂທີ່ດີທີ່ສຸດ
(DA650/525) ຂອງຕາຕະລາງກ່ອງ; (ຂ) ການວິເຄາະ ROC ແລະ ການປະເມີນຜົນການກວດວິນິດໄສ. (ຄ) ຕາຕະລາງຄວາມສັບສົນສຳລັບການວິນິດໄສຄົນເຈັບປົກກະຕິ ແລະ ຄົນເຈັບມະເຮັງ. (ງ) ຄວາມອ່ອນໄຫວ, ຄວາມຈຳເພາະ, ຄ່າຄາດຄະເນໃນທາງບວກ (PPV), ຄ່າຄາດຄະເນທາງລົບ (NPV) ແລະ ຄວາມຖືກຕ້ອງຂອງວິທີການທີ່ພັດທະນາຂຶ້ນ.
ດັ່ງທີ່ສະແດງຢູ່ໃນຮູບທີ 2b, ພື້ນທີ່ພາຍໃຕ້ເສັ້ນໂຄ້ງ ROC (AUC = 0.9274) ທີ່ໄດ້ຮັບສຳລັບເຊັນເຊີທີ່ພັດທະນາຂຶ້ນສະແດງໃຫ້ເຫັນເຖິງຄວາມອ່ອນໄຫວ ແລະ ຄວາມຈຳເພາະສູງ. ດັ່ງທີ່ເຫັນໄດ້ຈາກຕາຕະລາງກ່ອງ, ຈຸດຕໍ່າສຸດທີ່ເປັນຕົວແທນຂອງກຸ່ມ DNA ປົກກະຕິບໍ່ໄດ້ແຍກອອກຈາກຈຸດສູງສຸດທີ່ເປັນຕົວແທນຂອງກຸ່ມ DNA ມະເຮັງ; ດັ່ງນັ້ນ, ການວິເຄາະການຖົດຖອຍໂລຈິດສະຕິກຈຶ່ງຖືກນໍາໃຊ້ເພື່ອແຍກຄວາມແຕກຕ່າງລະຫວ່າງກຸ່ມປົກກະຕິ ແລະ ກຸ່ມມະເຮັງ. ໂດຍໃຫ້ຊຸດຂອງຕົວແປເອກະລາດ, ມັນປະເມີນຄວາມເປັນໄປໄດ້ຂອງເຫດການທີ່ເກີດຂຶ້ນ, ເຊັ່ນ: ກຸ່ມມະເຮັງ ຫຼື ກຸ່ມປົກກະຕິ. ຕົວແປຕາມມີຄ່າຢູ່ລະຫວ່າງ 0 ແລະ 1. ດັ່ງນັ້ນ, ຜົນໄດ້ຮັບແມ່ນຄວາມເປັນໄປໄດ້. ພວກເຮົາໄດ້ກໍານົດຄວາມເປັນໄປໄດ້ຂອງການລະບຸມະເຮັງ (P) ໂດຍອີງໃສ່ ΔA650/525 ດັ່ງຕໍ່ໄປນີ້.
ບ່ອນທີ່ b=5.3533,w1=-6.965. ສຳລັບການຈັດປະເພດຕົວຢ່າງ, ຄວາມເປັນໄປໄດ້ທີ່ໜ້ອຍກວ່າ 0.5 ໝາຍເຖິງຕົວຢ່າງປົກກະຕິ, ໃນຂະນະທີ່ຄວາມເປັນໄປໄດ້ 0.5 ຫຼືສູງກວ່າ ໝາຍເຖິງຕົວຢ່າງມະເຮັງ. ຮູບທີ 2c ສະແດງໃຫ້ເຫັນຕາຕະລາງຄວາມສັບສົນທີ່ສ້າງຂຶ້ນຈາກການກວດສອບຄວາມຖືກຕ້ອງແບບປ່ອຍມັນໄວ້ຄົນດຽວ, ເຊິ່ງຖືກນໍາໃຊ້ເພື່ອກວດສອບຄວາມໝັ້ນຄົງຂອງວິທີການຈັດປະເພດ. ຮູບທີ 2d ສະຫຼຸບການປະເມີນຜົນການທົດສອບການວິນິດໄສຂອງວິທີການ, ລວມທັງຄວາມອ່ອນໄຫວ, ຄວາມຈຳເພາະ, ຄ່າຄາດຄະເນໃນທາງບວກ (PPV) ແລະ ຄ່າຄາດຄະເນທາງລົບ (NPV).
ເຊັນເຊີຊີວະພາບທີ່ອີງໃສ່ໂທລະສັບສະຫຼາດ
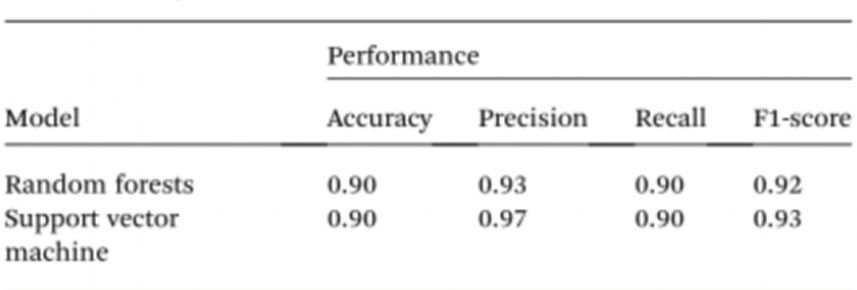
ເພື່ອເຮັດໃຫ້ການທົດສອບຕົວຢ່າງງ່າຍຂຶ້ນໂດຍບໍ່ຕ້ອງໃຊ້ເຄື່ອງວັດແທກແສງ, ນັກຄົ້ນຄວ້າໄດ້ໃຊ້ປັນຍາປະດິດ (AI) ເພື່ອຕີຄວາມໝາຍສີຂອງສານລະລາຍ ແລະ ຈຳແນກລະຫວ່າງບຸກຄົນປົກກະຕິ ແລະ ບຸກຄົນທີ່ເປັນມະເຮັງ. ດ້ວຍເຫດນີ້, ວິໄສທັດຄອມພິວເຕີຈຶ່ງຖືກນຳໃຊ້ເພື່ອແປສີຂອງສານລະລາຍ Cyst/AuNPs ໄປເປັນ DNA ປົກກະຕິ (ສີມ່ວງ) ຫຼື DNA ມະເຮັງ (ສີແດງ) ໂດຍໃຊ້ຮູບພາບຂອງແຜ່ນ 96-well ທີ່ຖ່າຍຜ່ານກ້ອງຖ່າຍຮູບໂທລະສັບມືຖື. ປັນຍາປະດິດສາມາດຫຼຸດຜ່ອນຄ່າໃຊ້ຈ່າຍ ແລະ ປັບປຸງການເຂົ້າເຖິງໃນການຕີຄວາມໝາຍສີຂອງສານລະລາຍອະນຸພາກນາໂນ, ແລະ ໂດຍບໍ່ຕ້ອງໃຊ້ອຸປະກອນເສີມໂທລະສັບສະຫຼາດຮາດແວທາງແສງໃດໆ. ສຸດທ້າຍ, ສອງແບບການຮຽນຮູ້ຂອງເຄື່ອງຈັກ, ລວມທັງ Random Forest (RF) ແລະ Support Vector Machine (SVM) ໄດ້ຮັບການຝຶກອົບຮົມໃຫ້ສ້າງແບບຈຳລອງ. ທັງແບບ RF ແລະ SVM ໄດ້ຈັດປະເພດຕົວຢ່າງຢ່າງຖືກຕ້ອງເປັນບວກ ແລະ ລົບດ້ວຍຄວາມຖືກຕ້ອງ 90.0%. ນີ້ຊີ້ໃຫ້ເຫັນວ່າການນຳໃຊ້ປັນຍາປະດິດໃນການຮັບຮູ້ຊີວະພາບທີ່ອີງໃສ່ໂທລະສັບມືຖືແມ່ນເປັນໄປໄດ້ດີ.
ຮູບທີ 3.(ກ) ຊັ້ນເປົ້າໝາຍຂອງສານລະລາຍທີ່ບັນທຶກໄວ້ໃນລະຫວ່າງການກະກຽມຕົວຢ່າງສຳລັບຂັ້ນຕອນການເກັບກຳຮູບພາບ. (ຂ) ຕົວຢ່າງຮູບພາບທີ່ຖ່າຍໃນລະຫວ່າງຂັ້ນຕອນການເກັບກຳຮູບພາບ. (ຄ) ຄວາມເຂັ້ມຂອງສີຂອງສານລະລາຍ cyst/AuNPs ໃນແຕ່ລະບໍ່ຂອງແຜ່ນ 96-ບໍ່ທີ່ສະກັດອອກຈາກຮູບພາບ (ຂ).
ໂດຍການນໍາໃຊ້ Cyst/AuNPs, ນັກຄົ້ນຄວ້າໄດ້ພັດທະນາແພລດຟອມການຮັບຮູ້ແບບງ່າຍໆສໍາລັບການກວດຫາພູມສັນຖານ methylation ແລະເຊັນເຊີທີ່ສາມາດຈໍາແນກ DNA ປົກກະຕິຈາກ DNA ມະເຮັງເມື່ອໃຊ້ຕົວຢ່າງເລືອດຕົວຈິງສໍາລັບການກວດຫາມະເຮັງເມັດເລືອດຂາວ. ເຊັນເຊີທີ່ພັດທະນາຂຶ້ນໄດ້ສະແດງໃຫ້ເຫັນວ່າ DNA ທີ່ສະກັດຈາກຕົວຢ່າງເລືອດຕົວຈິງສາມາດກວດຫາ DNA ມະເຮັງຈໍານວນໜ້ອຍ (3nM) ໃນຄົນເຈັບມະເຮັງເມັດເລືອດຂາວໄດ້ຢ່າງວ່ອງໄວແລະມີປະສິດທິພາບດ້ານຄ່າໃຊ້ຈ່າຍພາຍໃນ 15 ນາທີ, ແລະສະແດງໃຫ້ເຫັນຄວາມຖືກຕ້ອງ 95.3%. ເພື່ອເຮັດໃຫ້ການທົດສອບຕົວຢ່າງງ່າຍຂຶ້ນໂດຍການລົບລ້າງຄວາມຕ້ອງການເຄື່ອງວັດແທກ spectrophotometer, ການຮຽນຮູ້ຂອງເຄື່ອງຈັກໄດ້ຖືກນໍາໃຊ້ເພື່ອຕີຄວາມສີຂອງສານລະລາຍແລະຈໍາແນກລະຫວ່າງບຸກຄົນປົກກະຕິແລະບຸກຄົນມະເຮັງໂດຍໃຊ້ຮູບຖ່າຍໂທລະສັບມືຖື, ແລະຄວາມຖືກຕ້ອງຍັງສາມາດບັນລຸໄດ້ເຖິງ 90.0%.
ເອກະສານອ້າງອີງ: DOI: 10.1039/d2ra05725e
ເວລາໂພສ: ວັນທີ 18 ກຸມພາ 2023
 中文网站
中文网站